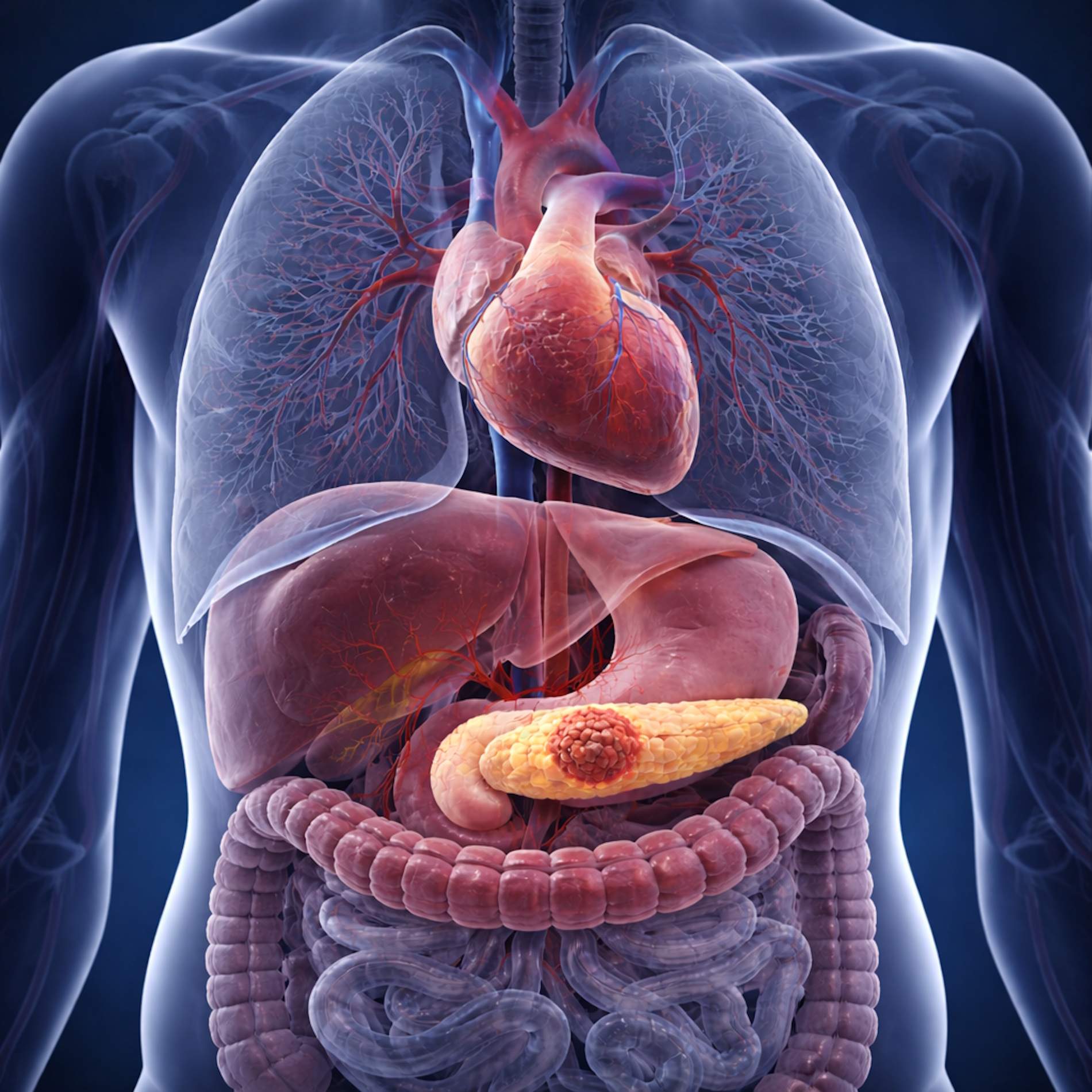
El càncer de pàncrees és un dels més temuts i letals que existeixen, agressiu i amb pitjor pronòstic. Aquest tipus de càncer sol diagnosticar-se tard i respon poc als tractaments actuals, que es basen sobretot en quimioteràpia tradicional i ofereixen una supervivència molt limitada. La supervivència en el càncer de pàncrees continua sent molt baixa, en part perquè la majoria dels casos es detecten quan el tumor ja no és operable. A més, a diferència d’altres càncers, hi ha molt poques opcions de teràpies dirigides o d’immunoteràpia. En aquest context, qualsevol millora té un gran impacte. Per això, notícies com la que explica La Vanguardia són encoratjadores. Un fàrmac anomenat daraxonrasib, que es pren per via oral un cop al dia, “marcarà un abans i un després en el tractament del càncer de pàncrees; és l’inici de l’era de les teràpies dirigides” per a una malaltia que fins ara s’ha tractat amb quimioteràpia, explica al diari barceloní Jaume Capdevila, del Vall d’Hebron Institut d’Oncologia (VHIO), que ha coordinat la participació de l’hospital barceloní en l’assaig clínic internacional.
L’estudi sobre el daraxonrasib (també anomenat RMC-6236) en càncer de pàncrees metastàtic ha estat liderat per Revolution Medicines, una companyia biotecnològica nord-americana amb seu a Redwood City (Califòrnia), especialitzada en teràpies dirigides contra mutacions RAS. En l’assaig clínic hi han participat 501 pacients dels Estats Units, Europa i el Japó. L’estudi ha comptat amb la implicació de quatre hospitals espanyols: el Vall d’Hebron de Barcelona, el Clínic Universitari de València, el Doce de Octubre de Madrid i la Clínica Universitat de Navarra. Tots els participants patien càncer de pàncrees amb metàstasi i ja havien rebut tractament amb quimioteràpia. Aproximadament la meitat van continuar amb aquest tractament, mentre que l’altra meitat el va substituir pel daraxonrasib.
Una nova via terapèutica
El més destacat és que aconsegueix duplicar la supervivència dels pacients, tant en termes de temps de vida com en el període en què la malaltia no progressa. A més, es tracta d’una teràpia més dirigida, que actua de manera més específica sobre el tumor i, per tant, podria tenir menys efectes secundaris que els tractaments convencionals. El càncer de pàncrees ha quedat al marge de moltes innovacions que sí que han funcionat en altres tumors, com la immunoteràpia o les teràpies cel·lulars. Per això, aquest nou tractament no només millora els resultats actuals, sinó que obre una nova via terapèutica que podria transformar la manera d’abordar aquesta malaltia en el futur. Cal tenir en compte que el càncer de pàncrees és el setè més comú entre la població espanyola (en el 2025 va tenir 10.338 diagnòstics), però, en canvi, és el tercer que més morts causa, amb 8.140 morts en el 2023, segons informa la Societat Espanyola d’Oncologia Mèdica (SEOM), segons explica el diari, que ha consultat diferents oncòlegs que sostenen que el daraxonrasib augura un canvi en aquest escenari. El daraxonrasib no cura la malaltia en pacients amb metàstasi, però obre la via a una supervivència més llarga i amb una qualitat de vida millor.
Resultats esperançadors
Ha duplicat la supervivència en pacients amb càncer de pàncrees metastàtic en un assaig clínic de fase 3, passant d’una mediana de 6,7 mesos amb quimioteràpia a 13,2 mesos. Aquest inhibidor de les proteïnes RAS, mutades en més del 90% d’aquests tumors, redueix la mortalitat en un 60%. Tot i l’optimisme, els investigadors mantenen certa prudència, ja que el fàrmac encara es troba en fases d’estudi i caldrà confirmar els resultats amb més assajos clínics abans que es pugui aplicar de manera generalitzada. Segons els primers resultats anunciats per Revolution Medicines en un comunicat, s’ha registrat una reducció de la mortalitat del 60% en el grup tractat amb daraxonrasib. És a dir, per cada 100 pacients tractats amb quimioteràpia que han mort durant l’assaig clínic, 60 han sobreviscut amb l’inhibidor de RAS. Pel que fa als efectes secundaris, Revolution Medicines només ha avançat que en l’assaig clínic “el daraxonrasib ha estat generalment ben tolerat, amb un perfil de seguretat manejable, i no s’hi han detectat nous senyals de seguretat”. L’efecte advers més comú reportat en assaigs anteriors amb menys pacients són les erupcions cutànies, seguides d’úlceres bucals, diarrea, nàusees i vòmits.
Com actua el fàrmac?
La clau d’aquest avenç és que el fàrmac actua sobre el gen KRAS, una mutació molt freqüent en el càncer de pàncrees i responsable del creixement tumoral. Durant dècades, aquest gen s’havia considerat pràcticament “intocable” des del punt de vista farmacològic, ja que era molt difícil de bloquejar amb medicaments. El fet que ara s’hagi aconseguit inhibir-lo de manera efectiva representa un canvi important en la recerca oncològica. Les mutacions de les proteïnes RAS són el motor de més del 90% dels càncers de pàncrees (més exactament, dels adenocarcinomes de pàncrees, que representen gairebé la totalitat dels càncers que s’inicien en aquest òrgan). També apareixen en prop del 40% dels càncers colorectals, el 30% dels de tiroide i el 25% dels de pulmó, entre d’altres tumors, de manera que els fàrmacs inhibidors de RAS poden aportar beneficis més enllà del càncer de pàncrees.
Quan podria estar al mercat?
Els resultats detallats de l’assaig de fase 3 es presentaran a la comunitat científica en el congrés de la Societat Americana d’Oncologia Mèdica, que se celebrarà a finals de maig, segons ha informat la companyia. Revolution Medicines està intentant agilitzar el procés, a través de designacions prioritàries de la FDA i avals especials per accelerar la revisió. “Ens estem movent amb urgència cap a la presentació [d’aquestes dades] a les autoritats reguladores globals”, declara en el comunicat Mark Goldsmith, conseller delegat de Revolution Medicines. Als Estats Units, l’Administració d’Aliments i Fàrmacs (FDA) ha atorgat al daraxonrasib el Segell de Prioritat Nacional, una nova qualificació destinada a accelerar l’aprovació de teràpies prioritàries.
La companyia ha obtingut la designació de Teràpia Innovadora (Breakthrough Therapy), revisió prioritària i un Commissioner’s National Priority Voucher (CNPV), que redueix el temps de revisió estàndard de 10-12 mesos a només 6 mesos o menys. Tenen previst presentar la sol·licitud d’aprovació (BLA) a la FDA immediatament després dels resultats positius de fase 3 de l’assaig RASolute 302, amb un segell prioritari per a necessitats mèdiques no cobertes en el càncer de pàncrees metastàtic. L’objectiu és portar el fàrmac al mercat tan aviat com sigui possible per als pacients amb mutacions RAS (el 90% dels casos), duplicant la supervivència i millorant la qualitat de vida en comparació amb la quimioteràpia estàndard, atesa la urgència d’aquest càncer letal.