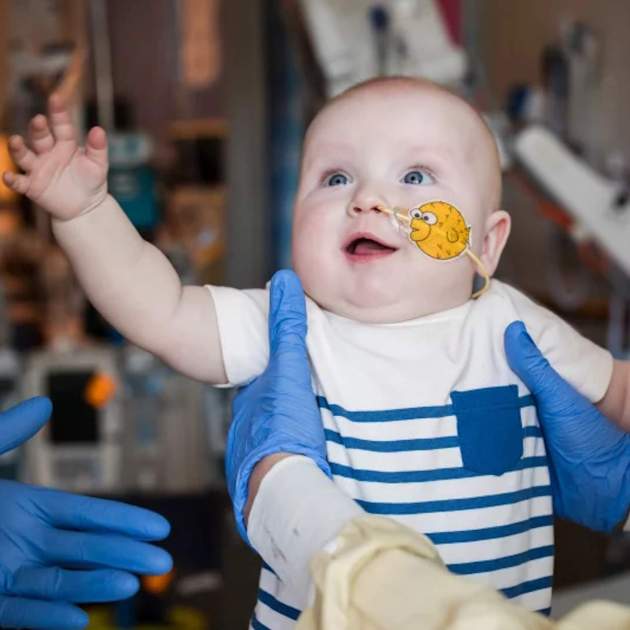
KJ Muldoon es un bebé de Pensilvània de menos de un año que nació con una patología metabólica muy rara e incurable, conocida como deficiencia grave de carbomoil fosfato sintetasa 1(CPS1). Esta enfermedad, que afecta uno de cada 1,3 millones de nacimientos, impide que su cuerpo convierta el amoníaco en urea, lo cual provoca una acumulación tóxica de amoníaco que puede causar daños severos en el cerebro, el hígado e incluso la muerte. Los síntomas suelen aparecer poco después del nacimiento y, en casos graves como el de KJ, la única solución a largo plazo suele ser un trasplante de hígado, y él era demasiado pequeño y frágil para esta intervención. Pero a veces, la medicina hace milagros, y el KJ ha hecho historia al convertirse en la primera persona tratada con una terapia genética personalizada, mediante edición genética CRISPR, desarrollada específicamente para él en el Hospital de Niños de Filadelfia (CHOP) y Penn Medicine. El caso de KJ, publicado este jueves en la The New England Journal of Medicine, supone un gran avance médico pionero en la medicina personalizada y en la aplicación del CRIPR para enfermedades ultra-raras, y abre la puerta a desarrollar tratamientos "hechos a medida" en tiempo récord para pacientes con mutaciones únicas que no disponen de opciones de curación.
Carrera contra reloj
Después del diagnóstico poco después del nacimiento de KJ en agosto del 2024, un equipo multidisciplinar del CHOP inició una carrera contra el reloj y en menos de seis meses consiguió crear la terapia exclusiva para el bebé y probar la eficacia y seguridad en células humanas y un modelo animal. En este tiempo también se consiguió que la FDA, la agencia reguladora de los medicamentos en los EE.UU., aprobara su aplicación. Así, KJ, que en aquel momento tenía entre seis y siete meses, pudo convertirse en el primer caso del mundo que ha podido beneficiarse de esta terapia génica con CRISPR para salvarse de una grave mutación genética única.
¿Qué es la CRISP?
La edición genética CRISPR es una revolucionaria técnica de biología molecular que permite modificar de manera precisa, eficiente y sencilla el ADN de organismos vivos. El término CRISPR corresponde al acrónimo en inglés de Clustered Regularly Interspaced Short Palindromic Repeats, que significa "repeticiones palindrómicas cortas agrupadas y regularmente inter espaciadas". Con este sistema, los científicos pueden editar genes en cualquier célula. La herramienta actúa como unas "tijeras moleculares" que cortan el ADN en el lugar deseado, y a partir de este corte, es posible eliminar (inactivar) genes, introducir nuevas secuencias o corregir mutaciones. En el caso de KJ, se utilizó una variante de CRISPR conocida cm en edición de bases (base editing) que permite cambiar una sola letra del ADN sin cortar completamente la doble hélice, lo cual reduce el riesgo de errores o efectos secundarios. El tratamiento CRISPR fue diseñado de manera personalizada para que el sistema de edición genética localizara y corrigiera únicamente la mutación concreta de KJ en el gen CPS1 (carbamoil fosfato sintetasa 1).
Miles de millones de editores genéticos
La terapia consistió en la administración de miles de millones de editores genéticos microscópicos (instrucciones genéticas encapsuladas en nanopartículas de grasa), que se administraron a través de tres infusiones intravenosas que transportaron los componentes de la edición genética del tratamiento directamente en el hígado, donde la edición CRISPR corrigió el error en el ADN. El bebé recibió la primera dosis entre los seis y siete meses de edad, y posteriormente otras dos dosis más. KJ toleró bien el tratamiento, sin complicaciones graves. La primera dosis fue baja y tuvo poco impacto, pero las siguientes dos consiguieron mejoras notables y los resultados son muy prometedores: el bebé está creciendo bien, ha podido aumentar la cantidad de proteína en su dieta y ha reducido la medicación necesaria para controlar sus niveles de amoníaco.
Los médicos son cautos y no hablan todavía de "curación", consideran que la terapia ha transformado su enfermedad de una forma grave en una más leve, y KJ sigue bajo observación médica estricta. "Es pronto para hablar de cura (...). Todavía estamos en una etapa muy inicial. Sabemos que todavía tenemos mucho a aprender de él", explicó la doctora Rebecca Ahrens-Nicklas, responsable del caso, que no puede esconder que el caso "es realmente emocionante" y que "demuestra el potencial que tenemos: que realmente podemos abrir la puerta a estos tratamientos transformadores para pacientes que no tienen otra opción. Las posibilidades son prácticamente ilimitadas", afirma Ahrens-Nicklas.