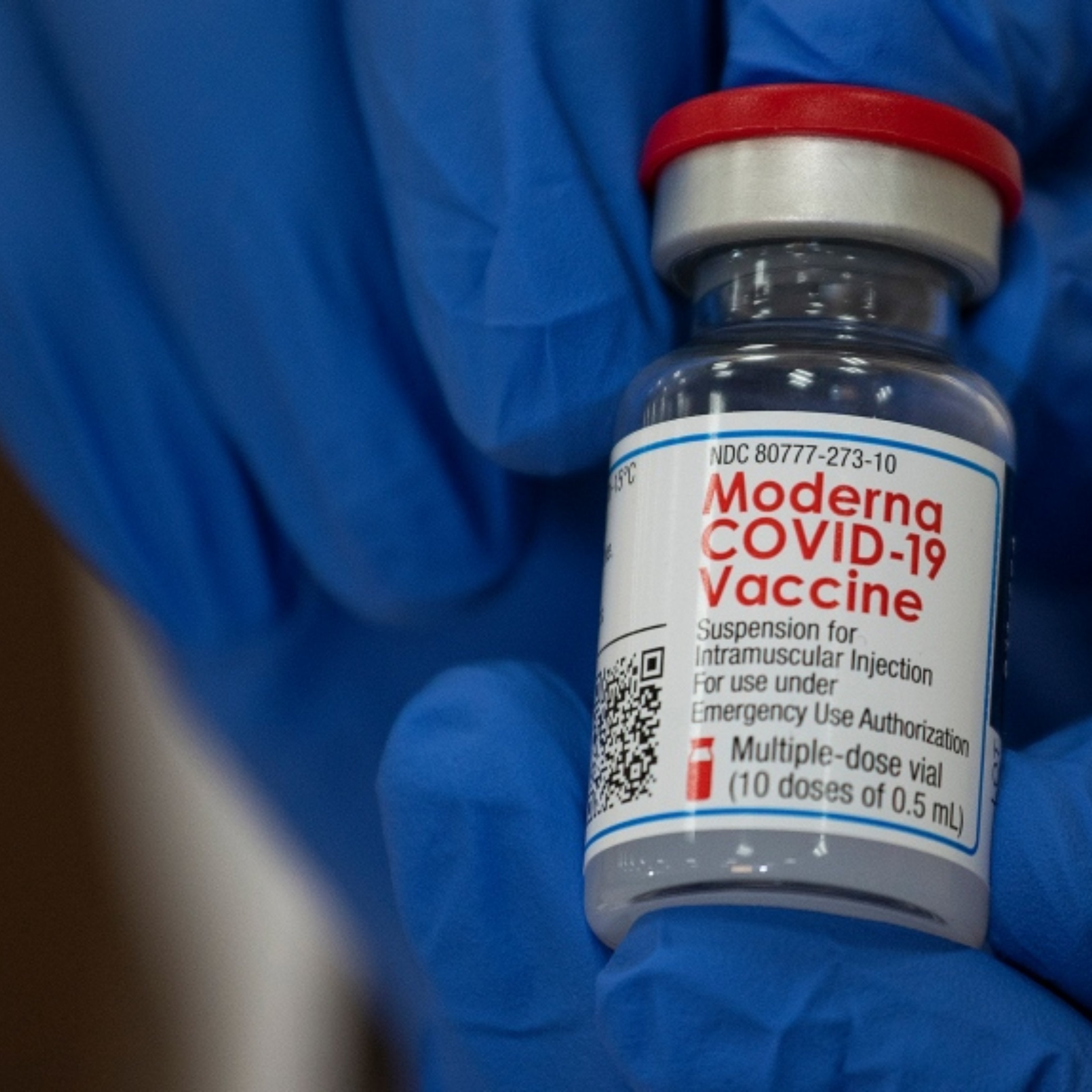
A finales de este mes de enero llegará a España una nueva vacuna creada para hacer frente al SARS-CoV-2, la de Moderna, una empresa de Cambridge en Massachusetts, desarrollada junto con el Instituto Nacional de Alergias y Enfermedades Infecciosas de Estados Unidos.
Al igual que la de Pfizer, se ha desarrollado mediante la tecnología del ARN Mensajero, diseñada para dirigir las células del cuerpo a producir proteínas intracelulares, de membrana o secretadas que pueden tener un beneficio terapéutico o preventivo y tienen el potencial de abordar un amplio espectro de enfermedades.
La vacunación de la vacuna de Moderna ya ha comenzado en Estados Unidos. Tal y como ha informado la propia compañía en un estudio publicado en The New England Journal of Medicine, los resultados provisionales de seguridad y eficacia primaria del ensayo de fase 3 de la vacuna –de dos dosis de 100 μg administrada con 28 días de diferencia– fue bien tolerado y demostró una eficacia del 94,1% contra la Covid-19. El estudio de fase 3, conocido como el estudio COVE, inscribió a más de 30.000 participantes en los Estados Unidos.
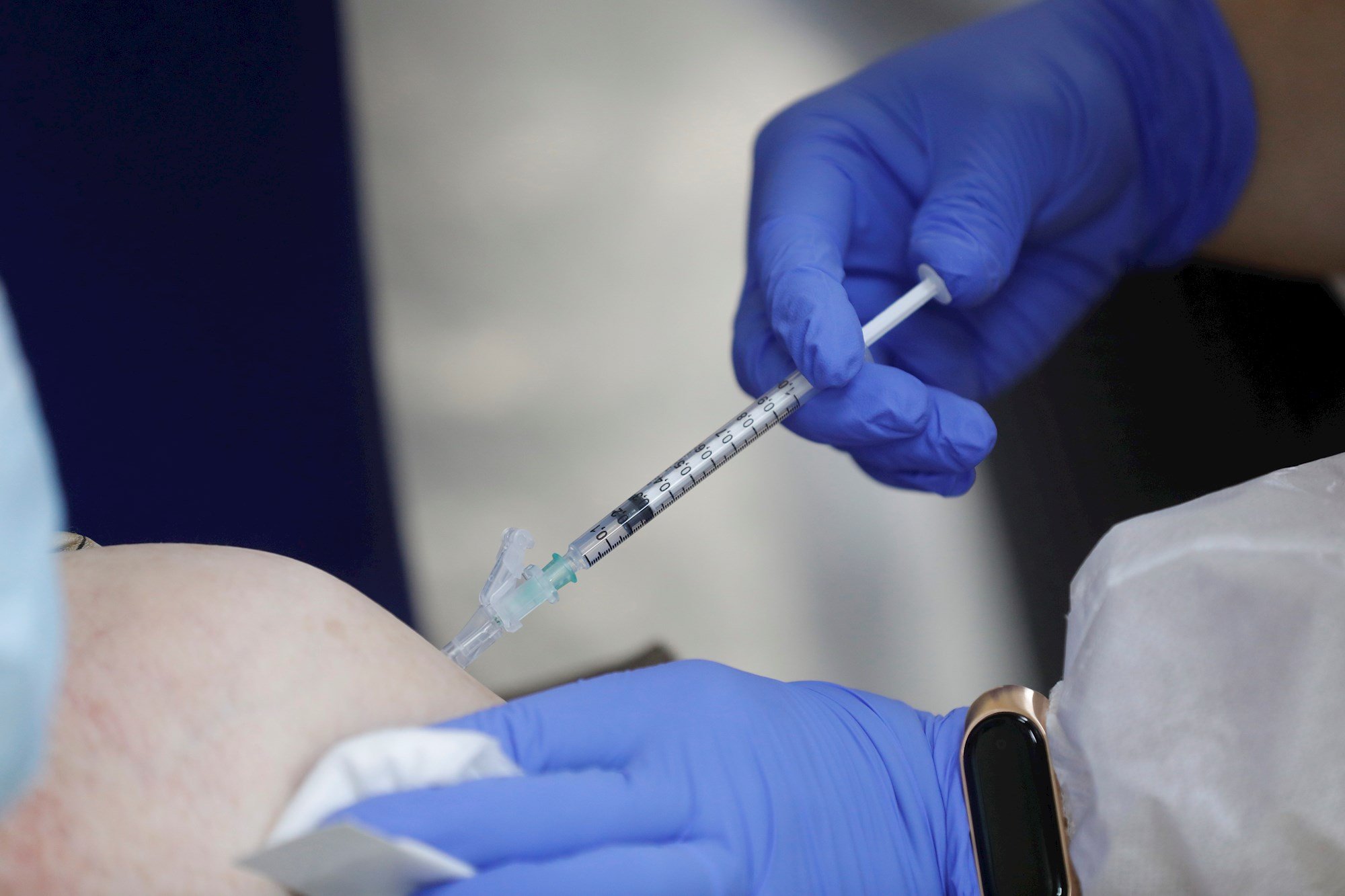 Las pruebas de la vacuna de Moderna han ofrecido un éxito del 94%
Las pruebas de la vacuna de Moderna han ofrecido un éxito del 94%
El criterio de valoración principal se basó en el análisis de los casos de Covid-19 confirmados y adjudicados a partir de dos semanas después de la segunda dosis de vacuna. Este análisis final se basó en 196 casos, de los cuales se observaron 185 casos de Covid-19 en el grupo de placebo frente a 11 casos observados en el grupo de vacuna Moderna Covid-19, lo que corresponde a una eficacia de la vacuna del 94,1%.
Un criterio de valoración secundario analizó los casos graves de Covid-19 e incluyó 30 casos graves (como se define en el protocolo del estudio) en este análisis. Los 30 casos ocurrieron en el grupo placebo y ninguno en el grupo vacunado. Hasta la fecha, hubo una muerte relacionada con Covid-19 en el estudio, que ocurrió en el grupo de placebo.
Entre estos participantes, la edad media fue de 51,4 años, el 47,3% eran mujeres, el 24,8% eran mayores de 65 años y el 16,7% tenían menos de 65 años pero tenían enfermedades crónicas de alto riesgo que los ponen en mayor riesgo de Covid grave, como diabetes, obesidad severa y enfermedades cardíacas. Los participantes de comunidades de color representaron el 37% de la población del estudio, similar a la diversidad de los Estados Unidos. Esto incluyó a un 20,5% de participantes que se identificaron como hispanos o latinos y un 10,2% de participantes que se identificaron como negros o afroamericanos.
Las reacciones adversas solicitadas más comunes después de la serie de dos dosis fueron el dolor en el lugar de la inyección (86%). Los eventos adversos sistémicos solicitados ocurrieron con más frecuencia en el grupo de la vacuna Moderna Covid-19 (54,9% y 79,4%) que en el grupo de placebo (42,2% y 36,5%) después de la primera y la segunda dosis respectivamente y fueron más comúnmente dolor de cabeza, fatiga y mialgia. Si bien la mayoría de estas reacciones adversas fueron leves (grado 1) o moderadas (grado 2), hubo una mayor incidencia de reacciones graves (grado 3) en el grupo de vacuna Moderna Covid-19 después de la primera (2,9%) y la segunda (15,8%). La mayoría de las reacciones adversas locales solicitadas se produjeron en el primer o segundo día después de la inyección y, en general, persistieron durante una media de uno a dos días.
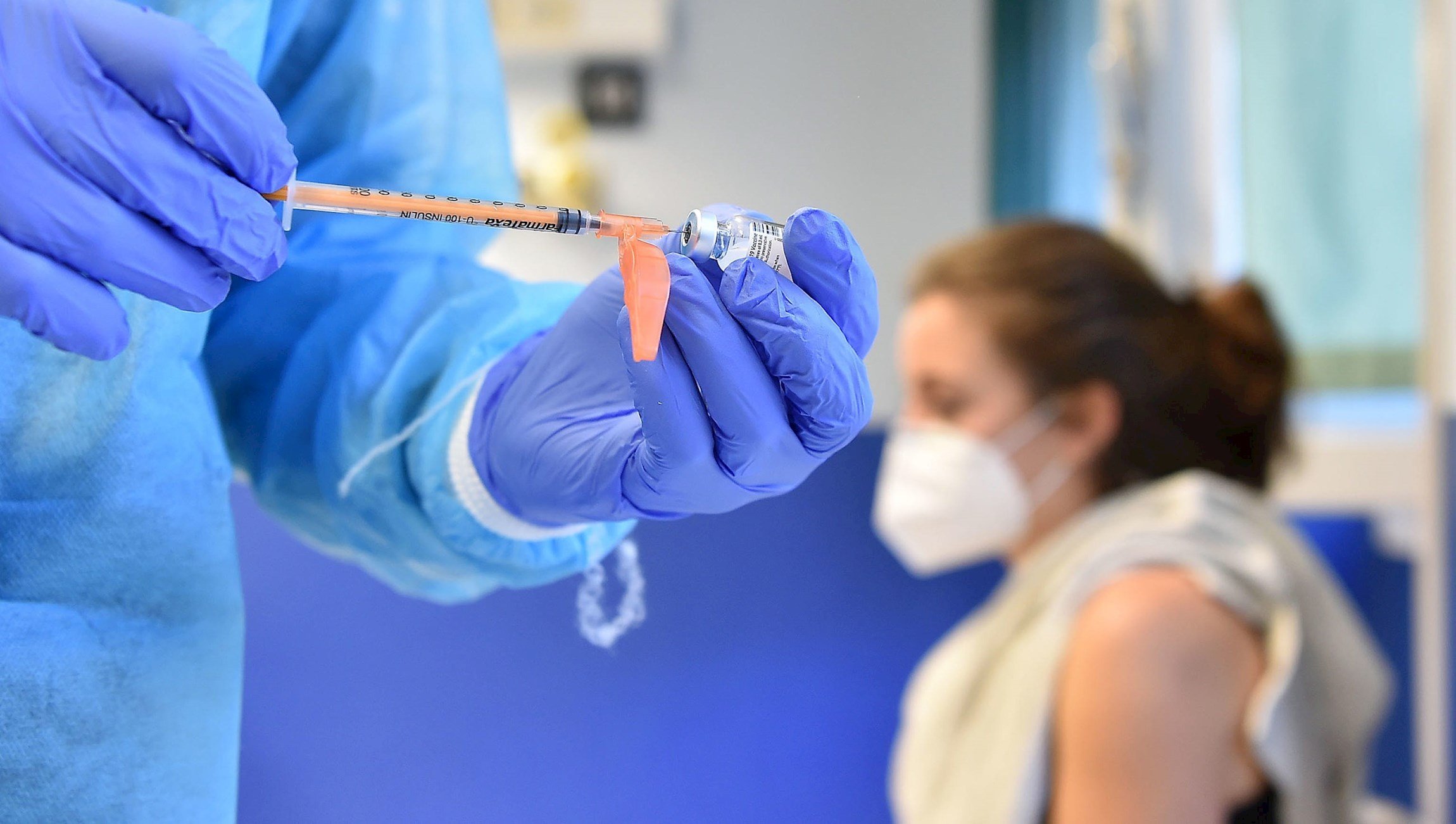 Los efectos negativos más comunes de la vacuna de Moderna han sido dolores de cabeza, fatiga y mialgia
Los efectos negativos más comunes de la vacuna de Moderna han sido dolores de cabeza, fatiga y mialgia
El estudio COVE de fase 3 está en curso y seguirá realizando un seguimiento de los participantes durante dos años. Los datos adicionales que se recopilarán incluirán un seguimiento de seguridad a más largo plazo, la duración de la protección contra Covid-19 y la eficacia contra la infección asintomática del SARS-CoV-2. Moderna también está realizando un estudio de Fase 2/3 de la vacuna Moderna Covid-19 en adolescentes de entre 12 y 18 años. Se planean estudios adicionales para evaluar la vacuna Moderna Covid-19 en mujeres embarazadas, niños menores de 12 años y aquellos en grupos de riesgo especiales, como los inmunodeprimidos.