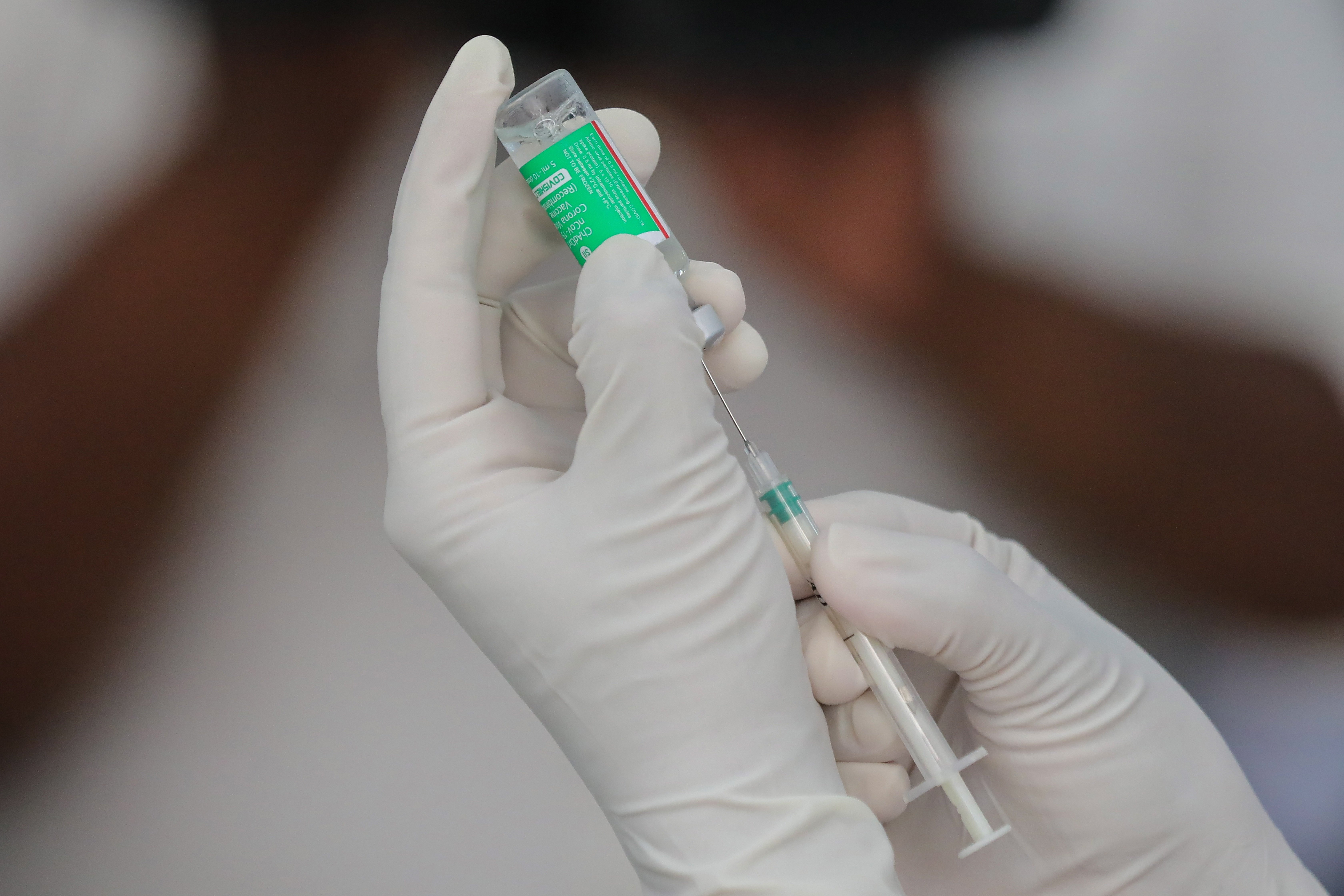
El Comité de Medicamentos Humanos (CHMP, por sus siglas en inglés) de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) ha recomendado otorgar la autorización condicional de comercialización a la vacuna de AstraZeneca contra la Covid-19 en personas de más de 18 años.
Esta es la tercera vacuna que la EMA ha recomendado para autorización después de la aprobación de las de Pfizer y Moderna. Según informa en un comunicado, el comité ha evaluado minuciosamente los datos sobre la calidad, seguridad y eficacia de la vacuna y ha recomendado por consenso que la Comisión Europea conceda una autorización de comercialización condicional formal. Esto garantizará a los ciudadanos de la UE que la vacuna cumple las normas de la UE y establece las salvaguardias, los controles y las obligaciones que sustentan las campañas de vacunación en toda la Unión.
"Con esta tercera opinión positiva, hemos ampliado aún más el arsenal de vacunas disponibles para los estados miembros de la UE para combatir la pandemia y proteger a sus ciudadanos. Como en casos anteriores, el CHMP ha evaluado rigurosamente esta vacuna y la base científica de nuestro trabajo respalda nuestro firme compromiso de salvaguardar la salud de los ciudadanos de la UE", ha señalado Emer Cooke, director Ejecutivo de la EMA.
Los resultados avalan la vacuna
Los resultados combinados de 4 ensayos clínicos en el Reino Unido, Brasil y Sudáfrica mostraron que la vacuna AstraZeneca es segura y eficaz para prevenir el coronavirus. Estos estudios involucraron a unas 24.000 personas en total. La mitad recibió la vacuna y la otra mitad recibió un placebo, ya sea una inyección ficticia u otra vacuna que no sea Covid.
La seguridad de la vacuna se ha demostrado en los cuatro estudios. Sin embargo, la Agencia ha basado su cálculo de qué tan bien funcionó la vacuna en los resultados de los estudios realizados en Reino Unido y en Brasil. Además, como la vacuna se administrará en dos dosis estándar y la segunda dosis debe administrarse entre 4 y 12 semanas después de la primera.
Los resultados de los estudios muestran una reducción del 59,5% en el número de casos sintomáticos de Covid-19 en personas que recibieron la vacuna (64 de 5258 recibieron Covid-19 con síntomas) en comparación con las personas que recibieron inyecciones de control (154 de 5210 recibieron la Covid con síntomas). Esto significa que la vacuna ha demostrado una eficacia de alrededor del 60% en los ensayos clínicos.
La incógnita, como funciona la vacuna en mayores de 55 años
La mayoría de los participantes en estos estudios tenían entre 18 y 55 años. Todavía no hay suficientes resultados en participantes mayores (mayores de 55 años) para proporcionar una cifra de qué tan bien funcionará la vacuna en este grupo.
Sin embargo, se espera protección, dado que se observa una respuesta inmune en este grupo de edad y en base a la experiencia con otras vacunas; dado que existe información confiable sobre seguridad en esta población, los expertos científicos de la EMA han considerado que la vacuna puede usarse en adultos mayores. Se espera más información de los estudios en curso, que incluyen una mayor proporción de participantes de edad avanzada.