La agencia del medicamento de los Estados Unidos (FDA) ha concedido este lunes la aprobación definitiva a la vacuna desarrollada por Pfizer y BioNTech para combatir la covid-19, así que este fármaco se convierte en el primero a superar el uso de emergencia que inicialmente se le otorgó al país norteamericano para agilizar el proceso de inmunización.
El permiso definitivo, aplicable para personas de más de 16 años, supone un "hito", como lo ha descrito la responsable en funciones de la Administración de Medicamentos y Alimentos (FDA) norteamericana, Janet Woodcock. En este sentido, confía en que este paso conceda una "confianza adicional" en una vacuna que cumple "los máximos estándares de seguridad, eficacia y calidad de fabricación".
El presidente de los Estados Unidos, Joe Biden, ha incidido en este enfoque, insistiendo en que "la aprobación del FDA tendría que tener una confianza mayor que esta vacuna es segura y efectiva". "Si no te has vacunado todavía, es el momento", ha proclamado en Twitter Biden, que tiene previsto, de hecho, recibir una tercera dosis de refuerzo de la vacuna de Pfizer.
Los EE.UU. apuestan por la tercera dosis
La noticia coincide con el hecho que la semana pasada, los responsables de Salud de los Estados Unidos expusieron que apuestan para inyectar una tercera dosis de la vacuna contra la covid-19. Así lo indicaron en un comunicado conjunto publicado por el Departamento de Salud norteamericano, que recogía la ACN, y que firmaban, entre otros, el asesor del presidente Joe Biden, el doctor Anthony Fauci, o el director del Centro de Control y Prevención de Enfermedades, Rochelle Walensky.
De esta manera, expusieron que las terceras dosis se podrían empezar a administrar a partir del 20 de septiembre a las personas que hace más de 8 meses que recibieron la segunda inyección. En todo caso, sin embargo, el plan espera la autorización del regulador, la FDA, que tiene que analizar los estudios presentados por Pfizer y Moderna sobre las terceras dosis.
¿Por qué ahora?
"Los datos disponibles dejan claro que la protección contra la infección de SARS-CoV-2 empieza a disminuir con el tiempo después de las dosis iniciales y, eso, junto con el variante delta, hace que empezamos a ver pruebas de una reducción de la protección en casos de enfermedad leve o moderada", afirmaba el comunicado.
Según los expertos de los Estados Unidos, "la actual protección contra una infección grave, hospitalización o muerte podría disminuir en los próximos meses, especialmente entre los que tienen mayor riesgo o se vacunaron hace más tiempo". "Por eso concluimos que una dosis de recordatorio será necesaria para maximizar la protección de las vacunas y alargarla", añadían.
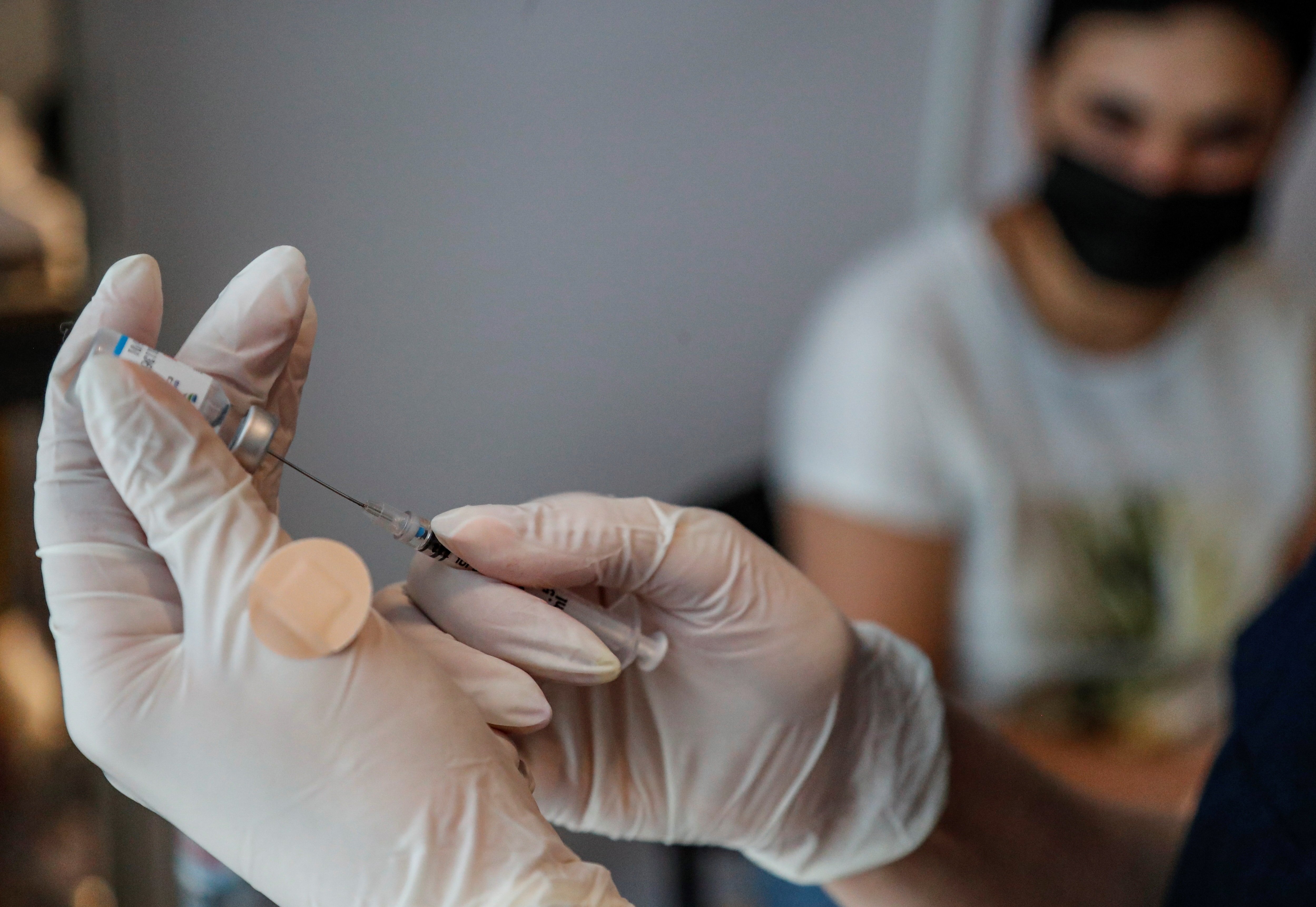
Imagen principal: una vacuna de Pfizer / Efe